Дайджест в области скрининга противоопухолевых препаратов с использованием трехмерных моделей опухоли

Эффективная система скрининга противоопухолевых препаратов должна быть максимально приближена по свойствам и организации к естественной опухоли. Такими основными моделями на сегодняшний день являются трехмерные (3D) клеточные культуры (в частности, опухолевые сфероиды).
В дайджесте описывается более детально о технологии трехмерного культивирования опухолевых сфероидов, а также о платформе формирования многоклеточных опухолевых сфероидов. Эти платформы предлагают биологически похожие структуры in vivo солидной опухоли, которые можно использовать для исследования сложных механизмов ответа опухоли на лекарства, что не позволяют более несовершенные двумерные (2D) платформы культивирования.
https://doi.org/10.3390/bios11110445
Трехмерная клеточная культура может быть достигнута с помощью двух подходов: независимо от закрепления и подхода типа закрепления. Первый обеспечивает эффективное поглощение питательных веществ через высокую поверхность, а второй обеспечивает стабильный рост клеток в биоматериалах, имитирующих опухолевый внеклеточный матрикс.
Опухолевые сфероиды дают возможность персонализированно подбирать подходящую терапию с учетом индивидуальных особенностей организма. А также при помощи рессеяния Бриллюэна стало возможно оценивать эффективность химиотерапии. Ученые из Франции создали сфероиды колоректального рака (клеточных линий HCT-116 и SW480), после чего измерили свдиг и уширение спектральны линий посредство оптического лазера. Исследователи обнаружили, что спектральные свойства излучения, прошедшие сквозь образец, отличаются от различных частей образца, что указывает на то, что механическое напряжение в центре сфероида больше, чем по краям.
https://journals.aps.org/prl/abstract/10.1103/PhysRevLett.122.018101
Одна из основных проблем при терапии онкологических заболеваний заключается в устойчивости к лекарственным препаратам. В недавних исследованиях стало известно, что плотность сфероида увеличивается за счет α5-#nbsp;и#nbsp;β1-интегринов при взаимодействии опухолевых клеток с внеклеточным матриксом, а также усиливаются контакты между опухолевыми клетками за счет E-кадгеринов, что создает определенный барьер для проникновения и распределения веществ, поступающих извне. (https://doi.org/10.1038/ncb0402-e83; https://doi.org/10.1242/bio.037051)
Российские ученые в коллаборации с коллегами из Венгрии и Финляндии разработали прибор, работающий на основе искусственного интеллекта. Система SpheroidPicker позволяет выделять сфероиды определенной формы и размера. «Особенность нашей разработки в том, что оператор может указать морфологические свойства, которые требуются для выбранных объектов, например, диапазон размеров. Перенос сфероид не влияет на морфологию и жизнеспособность клеток, поэтому в будущем SpheroidPicker может стать незаменимым инструментом для исследования лекарств против рака и новых протоколов лечения», — прокомментировал младший сотрудник Научно-учебной лаборатории искусственного интеллекта для вычислительной биологии ВШЭ Никита Мошков.
(https://www.hse.ru/news/505686398.html)
В следующем исследовании описывается комплексный анализ сфероидов, а также рост и структура сложных сфероидов с течением времени. Путем включения стромальных и опухолевых компонентов человека сложные сфероиды могут предоставить улучшенную модель опухолевого ответа на лекарственный препарат in vivo.
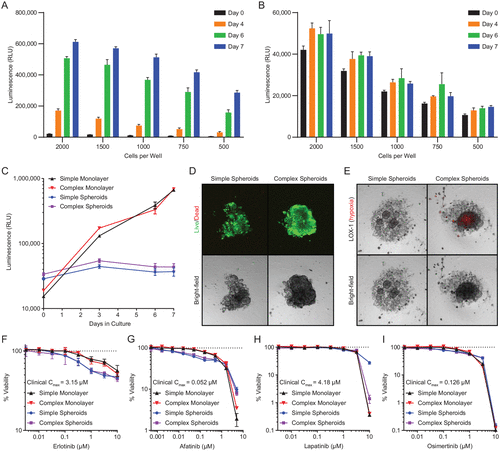
https://doi.org/10.1177/24725552211038362
Многие из существующих методов культивирования трехмерных сфероидов отнимают много времени и неэффективны и производят сфероиды неправильной формы, которые нелегко включить в биологические анализы. Трехмерные сфероиды, полученные с использованием платформы микролунок агарозы, функционируют как превосходная трехмерная модель in vitro для понимания степени проникновения, поглощения и распределения целевых грузов, таких как диагностические или терапевтические средства для выявления и лечения рака.
https://doi.org/10.1002/cpz1.199
Более того проиллюстрирована новая концепция использования сфероидов в качестве строительного блока в трехмерной биопечати для моделирования опухолей. Продемонстрирован будущий потенциал и проблемы формирования сфероидов, трехмерной биопечати и их комбинации, используемые для продвижения исследований рака.
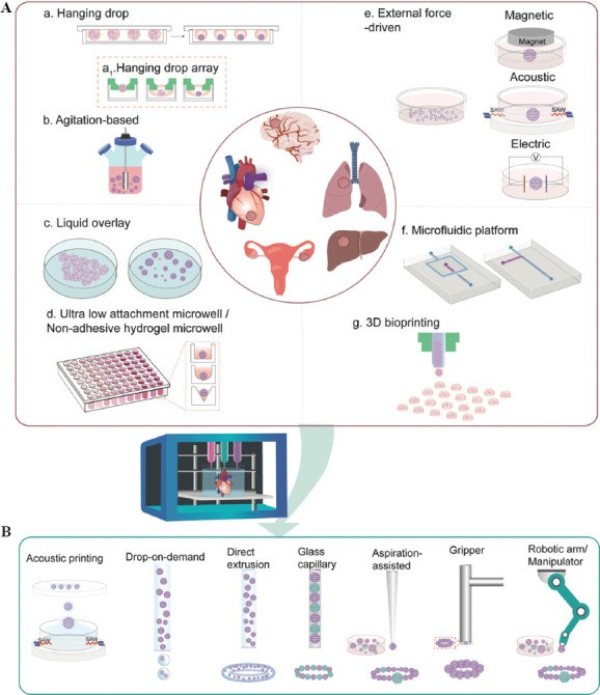
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8600307/
В недавнем исследовании ученые продемонстрировали ингибирование роста опухоли на примере опухолевых сфероидов рака предстательной железы. Никотинамидфосфорибозилтрансфераза (NAMPT) является ферментом, ограничивающим скорость синтеза никотинамидадениндинуклеотида (NAD), и участвует в пролиферации раковых клеток посредством регуляции путей производства энергии. Следовательно, ингибиторы NAMPT являются многообещающими лекарствами для лечения рака, ограничивая энергообеспечение опухолей.
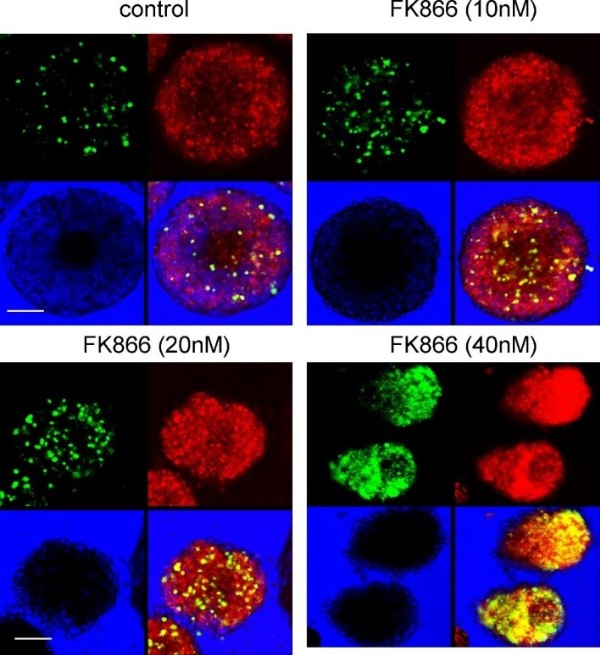
https://doi.org/10.1111/1440-1681.13452
В другом исследовании показали действие ингибиторов дезинтегрина A и металлопротеиназы 17 (ADAM17) в комбинации с цисплатином на 3-D моделях рака яичников. Ученые продемонстрировали, что ингибирование ADAM17 является многообещающей стратегией для лечения рака яичников.
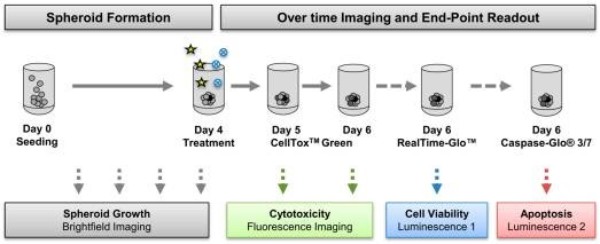
https://doi.org/10.3390/cancers13092039
Также на трехмерной модель сфероида рака легких с использованием человеческих клеток A549, заключенных в коллагеновый гель в секционированном микрофлюидном устройстве, была показана цитотоксическая активность богатого триптофаном пептида P1. Уничтожая опухолевые клетки, данный потенциальный противоопухолевый пептид при этом не затрагивал здоровые клетки.
https://doi.org/10.1002/adbi.201900285
Недавний прогресс описывается в отношении экспериментальных моделей рака, имеющих большее физиологическое и клиническое значение для скрининга лекарств, которые важны для успешной оценки клеточного ответа на лекарства. Рассматривается использование опухолевых сфероидов для изучения межопухолевой и внутриопухолевой гетерогенности и представляются перспективы клинического использования опухолевых сфероидов в рамках прецизионной медицины.
Гетерогенность внутри опухоли может быть еще одной проблемой для персонализированной медицины с использованием опухолевых биоптатов, полученных от пациентов. Это общая проблема отбора образцов из опухоли, поскольку популяции опухолевых клеток в разных частях одной и той же опухоли могут иметь разную лекарственную чувствительность.
https://doi.org/10.3390/cells8050470
Автор дайджеста:
Научно-клинический центр прецизионной и регенеративной медицины ИФМиБ КФУ
Информационный ресурс создан при поддержке грантом РНФ 21-74-10021