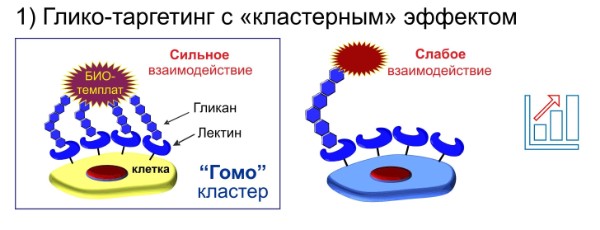
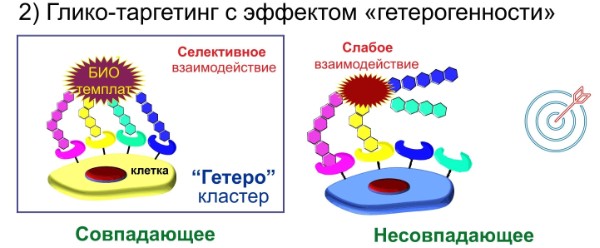
В настоящее время хорошо известно, что все без исключения живые клетки содержат массив ковалентно связанных моно- или олигосахаридов (гликанов). Находясь на внешней поверхности клеток и секретируемых макромолекул, гликаны участвуют в различных процессах живых систем: регуляция физико-химических свойств макромолекул, межклеточные взаимодействия, рост, дифференциация клеток и передача сигналов через мембрану. Аспарагин-связанные гликаны (N-гликаны) и их конъюгаты с белками или жирами играют особенно важную роль в таких явлениях, как врожденный иммунный ответ, адгезия клеток и распознавание клетками друг друга, которые основаны на механизмах распознавания образов. Важной составляющей данных механизмов являются эффекты мультивалентности и гетерогенности, свойственные гликанам.
Концепция «распознавания образов» гликанов
Несмотря на очевидную важность гликанов, прогресс в понимании их специфических функций ограничен сложностью и гетерогенностью данных соединений. В связи с этим огромными перспективами обладает синтез и изучение свойств гетерогенных гликопротеинов, несущих остатки нескольких различных гликанов. Именно с их помощью можно добиться большего подражания природным гликоконъюгатам клеточной стенки, которые представляют собой сложную комбинацию различных гликанов.
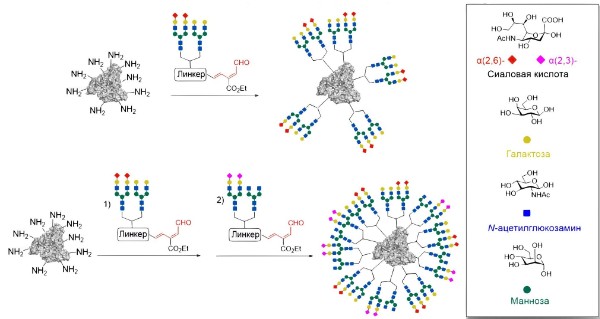
Разработана эффективная стратегия синтеза гетерогенных N-гликоальбуминов, со-держащих фрагменты двух или четырех различных N-гликанов и способных селективно распознавать раковые клетки. Для синтеза гетерогенных кластеров использован подход, основанный на первоначальном введении фрагментов двух различных N-гликанов в структуру азидсодержащего линкера и последующей иммобилизации N-гликаназидов на флуоресцентно меченый альбумин с помощью стратегии двух последовательных клик-реакций.
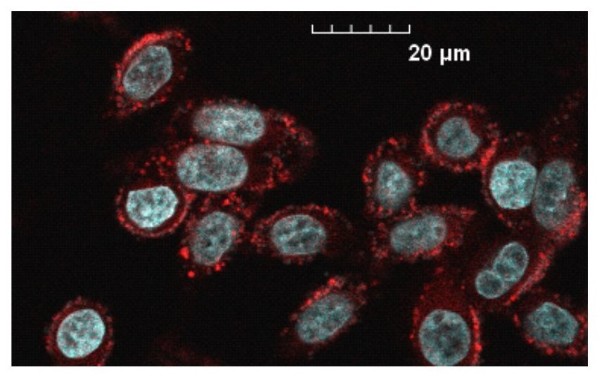
Исследование эффективности распознавания различных линий раковых клеток (HeLa, A549, HT29, BxPC3, MCF7, SW620) in vitro полученными гетерогенными гликоконъюгатами позволило выявить два гликокластера-лидера, на основе которых впервые синтезированы N-гликоальбумины c более высокой степенью гетерогенности, содержащие фрагменты четырех различных N-гликанов. Последние были вовлечены в цикл биологических исследований по оценке селективности их взаимодействия с различными линиями раковых клеток в экспериментах in vitro, а в отношении клеток SW620 проведена флуоресцентная визуализация ex vivo и in vivo в организмах модельных мышей.
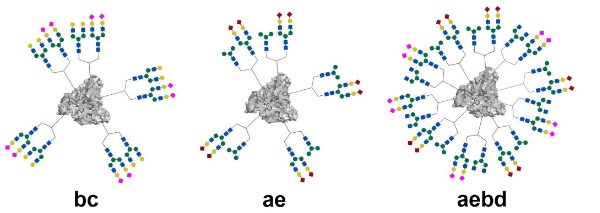
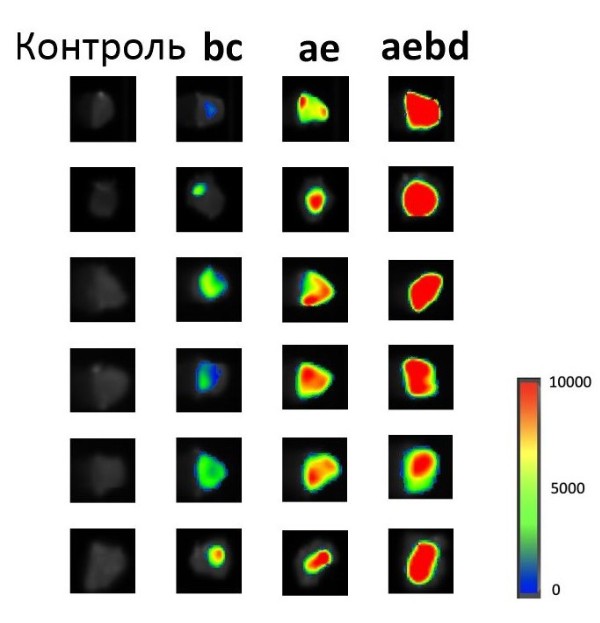

На эффективность распознавания раковых клеток N-гликоальбуминами влияют:
– структура углеводных фрагментов,
– количество углеводных фрагментов,
– их пространственное расположение в составе гликокластера,
– степень гетерогенности гликокластеров.
Результаты исследований свидетельствуют о селективном и эффективном распознава-нии раковых клеток N-гликоконъюгатами более высокого порядка, что крайне перспективно в области создания нового класса диагностических меток (или «трейсеров») на основе N-гликанов для обнаружения и визуализации целевых тканей и органов, для диагностики опухолей, а также при разработке систем адресной доставки лекарств.